Болезнь Паркинсона
 Болезнь Паркинсона (дрожательный паралич) – довольно часто встречающееся дегенеративное заболевание центральной нервной системы, которое проявляется комплексом двигательных нарушений в виде дрожания, замедленности движений, ригидности (неэластичности) мышц и неустойчивости тела.
Болезнь Паркинсона (дрожательный паралич) – довольно часто встречающееся дегенеративное заболевание центральной нервной системы, которое проявляется комплексом двигательных нарушений в виде дрожания, замедленности движений, ригидности (неэластичности) мышц и неустойчивости тела.
Заболевание сопровождается умственными и вегетативными расстройствами, изменениями личности. Для установления диагноза требуется наличие клинических симптомов и данные инструментальных методов исследования. Чтобы замедлить прогрессирование болезни и ухудшение состояния, больному с болезнью Паркинсона необходимо постоянно принимать лекарственные средства.
Дрожательный паралич развивается у 1% населения возрастом до 60 лет. Начало заболевания чаще всего припадает на возраст 55-60 лет, изредка выявляется у людей моложе 40 лет, и совсем редко – до 20 лет. В последнем случае это особая форма: ювенильный паркинсонизм.
Частота заболеваемости – 60-140 случаев на 100 000 населения. Мужчины болеют чаще, чем женщины, соотношение приблизительно 3:2.
Что это такое?
Болезнь Паркинсона – одно из наиболее распространенных нейродегенеративных заболеваний. Симптомы и признаки болезни Паркинсона весьма характерны: снижение двигательной активности, замедленность при ходьбе и движениях, дрожание конечностей в покое.
Обусловлено это поражением определенных структур головного мозга (черная субстанция, красное ядро), которые отвечают за выработку медиатора дофамина.
Причины возникновения
В основе болезни Паркинсона и паркинсонизма лежат уменьшение количества нейронов черной субстанции и формирование в них включений — телец Леви. Его развитию способствуют наследственная предрасположенность, пожилой и старческий возраст, воздействие экзогенных факторов. В возникновении акинетико-ригидного синдрома могут иметь значение наследственно обусловленное нарушение обмена катехоламинов в мозге или неполноценность ферментных систем, контролирующих этот обмен. Часто выявляется семейная отягощенность по этому заболеванию при аутосомно-доминантном типе наследования. Подобные случаи относят к болезни Паркинсона. Различные экзо– и эндогенные факторы (атеросклероз, инфекции, интоксикации, травмы) способствуют проявлению генуинных дефектов в механизмах обмена катехоламинов в подкорковых ядрах и возникновению заболевания.
Синдром паркинсонизма возникает в результате перенесенных острых и хронических инфекций нервной системы (клещевой и другие виды энцефалитов). Причинами болезни Паркинсона и паркинсонизма могут служить острые и хронические расстройства мозгового кровообращения, церебральный атеросклероз, сосудистые заболевания головного мозга, опухоли, травмы и опухоли нервной системы. Возможно развитие паркинсонизма вследствие лекарственных интоксикаций при длительном использовании препаратов фенотиазинового ряда (аминазин, трифтазин), метилдофы, некоторых наркотических средств – лекарственный паркинсонизм. Паркинсонизм может развиваться при острой или хронической интоксикации окисью углерода и марганца.
Основным патогенетическим звеном дрожательного паралича и синдрома паркинсонизма является нарушение обмена катехоламинов (дофамина, норадреналина) в экстрапирамидной системе. Дофамин выполняет самостоятельную медиаторную функцию в реализации двигательных актов. В норме концентрация дофамина в базальных узлах во много раз превышает его содержание в других структурах нервной системы. Ацетилхолин является медиатором возбуждения между полосатым телом, бледным шаром и черным веществом. Дофамин является его антагонистом, действуя тормозяще. При поражении черного вещества и бледного шара снижается уровень дофамина в хвостатом ядре и скорлупе, нарушается соотношение между дофамином и норадреналином, возникает расстройство функций экстрапирамидной системы. В норме импульсация модулируется в сторону подавления хвостатого ядра, скорлупы, черного вещества и стимулирования бледного шара.
При выключении функции черного вещества возникает блокада импульсов, поступающих из экстрапирамидных зон коры большого мозга и полосатого тела к передним рогам спинного мозга. В то же время к клеткам передних рогов поступают патологические импульсы из бледного шара и черного вещества. В результате усиливается циркуляция импульсов в системе альфа– и гамма-мотонейронов спинного мозга с преобладанием альфа-активности, что приводит к возникновению паллидарно-нигральной ригидности мышечных волокон и тремора – основных признаков паркинсонизма.
Что происходит?
Процесс дегенерации происходит в так называемой черной субстанции – группе клеток головного мозга, относящейся к подкорковым образованиям. Разрушение этих клеток приводит к снижению содержания дофамина. Дофамин – это вещество, с помощью которого осуществляется передача информации между подкорковыми образованиями о программируемом движении. Т. е. все двигательные акты как бы планируются в коре головного мозга, а реализуются с помощью подкорковых образований.
Снижение концентрации дофамина приводит к нарушению связей между нейронами, ответственными за движения, способствует повышению тормозных влияний. Т. е. выполнение двигательной программы затрудняется, замедляется. Кроме дофамина, на формирование двигательного акта влияют ацетилхолин, норадреналин, серотонин. Эти вещества (медиаторы) также играют роль в передаче нервных импульсов между нейронами. Дисбаланс медиаторов приводит к формированию неправильной программы движений, и моторный акт реализуется не так, как того требует ситуация. Движения становятся медленными, появляется дрожание конечностей в покое, нарушается тонус мышц.
Процесс разрушения нейронов при болезни Паркинсона не останавливается. Прогрессирование приводит к появлению все новых и новых симптомов, к усилению уже имеющихся. Дегенерация захватывает и другие структуры головного мозга, присоединяются умственные и психические, вегетативные расстройства.
Классификация
При формулировке диагноза учитывается преобладающий симптом. Исходя из этого, выделяют несколько форм:
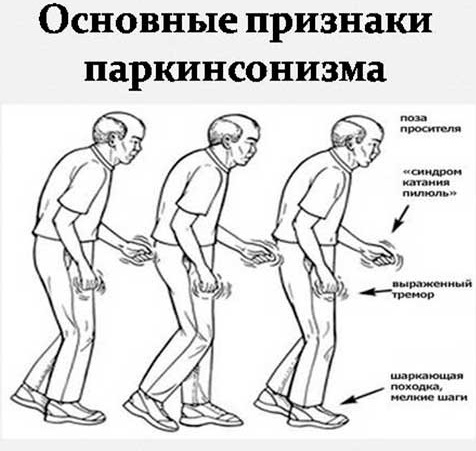
- Ригидно-брадикинетический вариант, для которого в наибольшей мере характерно повышение мышечного тонуса и нарушение двигательной активности. Таких больных, пока они ходят, легко узнать по «позе просителя», однако они быстро теряют способности к активному движению, перестают стоять и садиться, а вместо этого — приобретают инвалидность с пребыванием до конца жизни в обездвиженном состоянии;
- Дрожательно-ригидную форму, основными признаками которой являются дрожание и скованность движений;
- Дрожательную форму. Ее ведущий симптом, конечно, тремор. Ригидность выражена незначительно, двигательная активность особо не страдает.
Для оценки стадий болезни Парконсона широко применяется модифицированная шкала по Хен и Яру (Hoehn&Yahr), которая учитывает распространенность процесса и степень выраженности проявлений:
- стадия 0 – признаки заболевания отсутствуют;
- стадия 1 – односторонний процесс (вовлечены только конечности);
- стадия 1.5 – односторонний процесс с вовлечением туловища;
- стадия 2 – двусторонний процесс без нарушения равновесия;
- стадия 2.5 – начальные проявления двустороннего процесса с легкими нарушениями равновесия (при пробе толчка пациент делает несколько шагов, но возвращается в исходную позицию);
- стадия 3 – от начальных до умеренных проявлений двустороннего процесса с нестабильностью позы, самообслуживание сохранено, пациент физически независим;
- стадия 4 – тяжелая инвалидизация, сохранена способность стоять, ходить без поддержки, способность к прогулкам, элементы самообслуживания;
- стадия 5 – полная инвалидизация, беспомощность.
Трудоспособность и присвоение группы инвалидности зависят от того, насколько выражены двигательные расстройства, а также от профессиональной деятельности пациента (умственный труд или физический, работа требует точных движений или нет?). Между тем, при всем старании медиков и пациента инвалидность не проходит стороной, разница лишь в сроках ее наступления. Лечение, начатое на ранней стадии, может уменьшать выраженность клинических проявлений, однако не стоит думать, что больной вылечился – просто на некоторое время затормозился патологический процесс.
Когда человек уже практически прикован к постели, лечебные мероприятия, даже самые интенсивные, должного эффекта не дают. Знаменитая леводопа и та особо не обнадеживает в плане улучшения состояния, она лишь на короткое время замедляет прогрессирование болезни, а потом все возвращается на круги своя. Долго сдерживать болезнь на стадии выраженной симптоматики не получится, больной уже не покинет кровать, и обслуживать себя не научится, следовательно, будет до конца своих дней нуждаться в постоянной посторонней помощи.
Симптомы болезни Паркинсона
На ранних стадиях развития болезнь Паркинсона диагностировать сложно из-за медленного развития клинических симптомов. Она может манифестировать болью в конечностях, которую ошибочно можно связать с заболеваниями позвоночника. Нередко могут встречаться депрессивные состояния.
Основным проявлением паркинсонизма является акинетико-ригидный синдром, который характеризуется следующими симптомами:
- Тремор
Является довольно динамичным симптомом. Его появление может быть связано как с эмоциональным состоянием пациента, так и с его движениями. Например, тремор в руке может уменьшаться во время осознанных движений, и усиливаться при ходьбе или движении другой рукой. Иногда его может и не быть. Частота колебательных движений небольшая – 4-7 Гц. Они могут наблюдаться в руке, ноге, отдельных пальцах. Помимо конечностей, «дрожание» может отмечаться в нижней челюсти, губах и языке. Характерный паркинсонический тремор в большом и указательном пальцах напоминают «катание пилюль» или «счет монет». У некоторых пациентов он может возникать не только в покое, но и при движении, вызывая дополнительные трудности при приеме пищи или письме.
- Ригидность
Двигательные расстройства, вызванные акинезией, усиливаются за счет ригидности – повышения мышечного тонуса. При внешнем осмотре пациента она проявляется повышенным сопротивлением пассивным движениям. Чаще всего оно бывает неравномерным, что обуславливает появление феномена «зубчатого колеса» (возникает ощущение, что сустав состоит из зубчатых колес). В норме тонус мышц-сгибателей преобладает над тонусом мышц-разгибателей, поэтому ригидность в них выражена сильнее. Вследствие этого отмечаются характерные изменения позы и походки: туловище и голова таких пациентов наклонены вперед, руки согнуты в локтях и приведены к туловищу, ноги немного согнуты в коленях («поза просителя»).
- Брадикинезия (акинезия)
Представляет собой значительное замедление и обеднение двигательной активности, и является основным симптомом болезни Паркинсона. Она проявляется во всех группах мышц, но больше всего заметна на лице из-за ослабления мимической активности мышц (гипомимия). Из-за редкого мигания глаз, взгляд кажется тяжелым, пронзительным. При брадикинезии речь становится монотонной, приглушенной. Из-за нарушения глотательных движений может появиться слюнотечение. Истощается также мелкая моторика пальцев рук: пациенты с трудом могут совершать привычные движения, такие как застегивание пуговиц. При письме наблюдается преходящая микрография: к концу строки буквы становятся мелкими, неразборчивыми.
- Постуральная неустойчивость
Представляет собой особое нарушение координации движений при ходьбе, обусловленное утратой постуральных рефлексов, участвующих в поддержании равновесия. Этот симптом проявляется на поздней стадии заболевания. Такие пациенты испытывают некоторые трудности при изменении позы, смены направления движения и начале ходьбы. Если небольшим толчком вывести больного из равновесия, то он вынужден будет сделать несколько быстрых коротких шагов вперед или назад (пропульсия или ретропульсия), чтобы «догнать» центр тяжести тела и не потерять равновесие. Походка при этом становится семенящей, «шаркающей». Следствием этих изменений являются частые падения. Постуральная неустойчивость сложно поддается терапии, поэтому часто является причиной, по которой пациент с болезнью Паркинсона оказывается прикованным к постели. Двигательные расстройства при паркинсонизме нередко сочетаются и с другими нарушениями:
Психические нарушения:
- Когнитивные расстройства (деменция) — нарушается память, появляется замедленность взгляда. При тяжелом протекании заболевания возникают серьезные когнитивные проблемы — слабоумие, снижение познавательной деятельности, способность здраво рассуждать, выражать мысли. Эффективного способа замедления развития деменции нет, но клинические исследования доказывают, что применение Ривастигмина, Донепезила несколько снижают такие симптомы.
- Эмоциональные изменения — депрессия, она является самым первым симптомом болезни Паркенсона. Пациенты теряют уверенность в себе, боятся новых ситуаций, избегают общения даже с друзьями, появляется пессимизм, раздражительность. Возникае повышенная сонливость в дневное время, нарушается сон в ночное время, снятся кошмары, слишком эмоциональные мечты. Недопустимо использовать какие-либо препараты для улучшения сна без рекомендации врача.
Вегетативные нарушения:
- Ортостатическая гипотензия — снижение артериального давления при смене положения тела (когда человек резко встает), это приводит к снижению кровоснабжения мозга, головокружению и иногда к обмороку.
- Учащение мочеиспускания или наоборот затруднения с процессом опорожнения мочевого пузыря.
- Расстройства ЖКТ связаны с нарушением моторики кишечника — запоры, связанные с инертностью, плохим питанием, ограничением питья. Также причиной запоров является прием препаратов от паркинсонизма.
- Снижение потоотделения и повышение сальности кожи — кожа на лице становится масляной, особенно в области носа, лба, головы (провоцирует возникновение перхоти). В некоторых случаях может быть наоборот, кожа становится слишком сухой. Обычное дерматологическое лечение улучшает состояние кожи.
Прочие характерные симптомы:
- Мышечные спазмы — из-за недостатка движения у больных (ригидностью мышц) возникают мышечные спазмы, чаще в нижних конечностях, для снижения частоты судорог помогает массаж, прогревание, растяжка.
- Проблемы с речью — трудности с началом разговора, монотонность речи, повторение слов, слишком быстрая или нечленораздельная речь наблюдается у 50% больных.
- Трудности с приемом пищи — это связано с ограничением двигательной активности мышц, отвечающих за жевание, глотание, происходит повышенное слюноотделение. Задержка слюны в полости рта может приводить к удушью.
- Половая дисфункция — депрессия, прием антидепрессантов, ухудшение кровообращения приводят к нарушениям эрекции, снижению сексуального влечения.
- Быстрая утомляемость, слабость — повышенная усталость обычно усиливается к вечеру и связана с проблемами начала и окончания движений, она также может быть связана с депрессией, бессонницей. Установление четкого режима сна, отдыха, сокращение физической активности помогают снизить степень утомления.
- Мышечные боли — ломота в суставах, мышцах вызваны нарушением осанки и ригидностью мышц, использование леводопы снижают такие боли, также помогают некоторые виды упражнений.
Диагностика
Дабы диагностировать описываемый недуг сегодня разработаны унифицированные критерии, разделившие процесс диагностики на этапы. Начальный этап заключается в распознавании синдрома, следующий – в поиске проявлений, исключающих данное заболевание, третий – в выявления симптоматики, подтверждающей рассматриваемое заболевание. Практика показывает, что предложенные критерии диагностирования обладают высокой чувствительностью и довольно специфичны.
Первой ступенью в диагностировании болезни Паркинсона является распознавание синдрома с целью его разграничения с неврологической симптоматикой и психопатологическими проявлениями, сходной по ряду проявлений с истинным паркинсонизмом. Другими словами, начальный этап характеризуется проведением дифференциальной диагностики. Истинным паркинсонизм является при обнаружении гипокинезии в комбинации с минимум одним из ниже приведенных проявлений: ригидностью мускул, дрожанием покоя, постуральной неустойчивостью, не обусловленной первичными вестибулярными, зрительными, проприоцептивными и мозжечковыми расстройствами.
Следующий этап диагностирования болезни Паркинсона предусматривает исключение иных недугов, которые проявляются синдромом паркинсонизма (так называемые отрицательные критерии диагностики паркинсонизма).
Различают следующие критерии исключения рассматриваемого недуга:
- анамнестические свидетельства о повторных инсультах со ступенчатым прогрессированием симптоматики паркинсонизма, неоднократное травмирование мозга либо достоверный энцефалит;
- применение нейролептиков перед началом недуга;
- окулогирные кризы;продолжительная ремиссия;
- надъядерный прогрессирующий парез взора;
- односторонняя симптоматика, длящаяся больше трехлетнего периода;
- мозжечковые проявления;
- раннее возникновение симптоматики выраженной вегетативной дисфункции;
- симптом Бабинского (аномальное ответное реагирование на механическое раздражение стопы);
- наличие опухолевого процесса в мозге;
- раннее возникновение выраженной деменции;
- отсутствие результата от употребления больших дозировок Леводопы;
- наличие открытой гидроцефалии;
- отравление метил-фенил-тетрагидропиридином.
Диагностика болезни Паркинсона последний шаг – это поиск симптоматики, подтверждающей рассматриваемую патологию. Дабы достоверно диагностировать описываемое расстройство, необходимо выявить минимум три критерия из приведенных ниже:
- наличие дрожания покоя;
- дебют недуга с односторонней симптоматики;
- устойчивая асимметрия, характеризуемая более явными проявлениями на половине туловища, с которой дебютировало заболевание;
- хорошее реагирование на применение Леводопы;
- присутствие выраженной дискинезии, вызванной приемом Леводопы;
- прогрессирующее протекание недуга;
- сохранение результативности Леводопы на протяжении минимум 5 лет; продолжительное течение недуга.
Важное значение в диагностировании болезни Паркинсона играет анамнез и осмотр врачом-неврологом.
В первый черед, невролог выясняет местность обитания пациента, во сколько лет дебютировало заболевание и какими проявлениями, известны ли случаи возникновения рассматриваемого недуга в семье, предшествовали ли патологии различные травмы мозга, интоксикации, затихает ли дрожание при покое, какие появились двигательные нарушения, симметричны их проявления, может ли самостоятельно обслуживать себя, справляется с повседневными делами, появились ли расстройства потоотделения, сдвиги в эмоциональном настрое, нарушения сновидения, какие принимал препараты, есть ли результат их воздействия, принимал ли Леводопу.
После сбора данных анамнеза невролог оценивает походку пациента и позу его тела, а также свободу двигательных актов в конечностях, мимику, наличие дрожания в покое и при нагрузке, выявляет наличие симметрии проявлений, определяет речевые расстройства и дефекты почерка.
Кроме сбора данных и осмотра, обследование также должно включать инструментальное исследование. Анализы при диагностировании рассматриваемого недуга не специфичны. Они, скорее, несут вспомогательное значение. Дабы исключить иные хвори, которые протекают с симптоматикой паркинсонизма, определяют уровень концентрации глюкозы, содержание холестерина, печеночные ферменты, количество гормонов щитовидки, берут почечные пробы. Инструментальная диагностика болезни Паркинсона способствует выявлению ряда изменений свойственных паркинсонизму или иным недугам.
При помощи электроэнцефалографии можно обнаружить снижение в мозге электрической активности. Электромиография отображает частоту дрожания. Данный метод способствует раннему выявлению описываемой патологии. Позитронная эмиссионная томография также незаменима на дебютных этапах недуга еще до возникновения типичной симптоматики. Также проводится исследование, позволяющее обнаружить снижение продуцирования дофамина.
Нужно помнить, что всякий клинический диагноз бывает только возможным либо вероятным. Чтобы достоверно определить недуг необходимо проведение патоморфологического исследования.
Возможный паркинсонизм характеризуется наличием самое меньшее двух определяющих проявлений – это акинезия и дрожание или ригидность, прогрессирующим протеканием, отсутствием атипичной симптоматики.
Вероятный паркинсонизм характеризуется наличием аналогичных критериев, как и при возможном, плюс присутствием минимум двух из ниже следующих проявлений: явное улучшение от приема Леводопы, возникновение флюктуации двигательных функций или дискинезии, спровоцированные приёмом Леводопы, асимметричность проявлений.
Достоверный паркинсонизм характеризуется наличием аналогичных критериев, как и при вероятном, а также отсутствием олигодендроглиальных включений, присутствием разрушения пигментированных нейронов, выявленного посредством патоморфологического исследование, наличием телец Леви в нейронах.
Как выглядят люди с болезнью Паркинсона?
Для людей, страдающих болезнью Паркинсона (см. фото), характерна скованность всего тела, руки обычно прижаты к туловищу и согнуты в локтях, ноги расположены параллельно друг другу, тело немного наклонено вперёд, голова вытянута, как будто подпирается подушкой.
Иногда можно заметить лёгкое дрожание всего тела, особенно конечностей, головы, нижней челюсти, век. Из-за паралича мимических мышц лицо приобретает выражение «маски», то есть не выражает эмоций, спокойное, человек редко моргает или улыбается, взгляд надолго задерживается в одной точке.
Походка страдающих болезнью Паркинсона очень медленная, неуклюжая, шаги маленькие, неустойчивые, руки при ходьбе не двигаются, а остаются прижатыми к туловищу. Также отмечаются общая слабость, недомогание, депрессия.
Последствия
Последствия болезни Паркинсона весьма серьезные, и наступают они тем быстрее, чем позднее начинается лечение:
- Акинезию, то есть невозможность совершать движения. Но, стоит отметить, что полная обездвиженность наступает редко и в самых запущенных случаях.
- Чаще люди сталкиваются с ухудшением работы двигательного аппарата различной степени выраженности.
- Запоры, которые иногда приводят даже к летальному исходу. Это происходит из-за того, что больные становятся не в состоянии употреблять пищу и воду в должном количестве, чтобы стимулировать нормальную работу кишечника.
- Раздражение зрительного аппарата, что связано с сокращением числа мигательных движений век до 4 раз за минуту. На фоне этого часто появляются конъюнктивиты, воспаляются веки.
- Себорея – ещё одно осложнение, часто преследующее людей с болезнь Паркинсона.
- Деменция. Она выражается в том, что человек становится замкнутым, неактивным, подвержен депрессиям и эмоциональной бедности. Если присоединяется деменция, то прогноз течения болезни существенно ухудшается.
Как лечить болезнь Паркинсона?
Больной, у которого обнаружены начальные симптомы болезни Паркинсона требует внимательного лечения с индивидуальным курсом, связанно это с тем, что упущенное лечение приводит к серьезным последствиям.
Основной задачей в лечении служат:
- как можно дольше поддерживать двигательную активность у больного;
- разработка специальной программы физических упражнений;
- медикаментозная терапия.
Врач при выявлении заболевания и ее стадии назначает препараты при болезни Паркинсона, соответствующие этапу развития синдрома:
- Вначале эффективны таблетки амантадин, которые стимулирует продукцию дофамина.
- На первом этапе также эффективны агонисты дофаминовых рецепторов (мирапекс, прамипексол).
- Лекарство леводопа в сочетании с другими препаратами назначают в комплексной терапии на более поздних стадиях развития синдрома.
Базовым лекарственным средством, способным затормозить развитие синдрома Паркинсона является Леводопа. Следует отметить, что у препарата имеется ряд побочных эффектов. До ведения в клиническую практику данного средства единственным значимым методом лечения являлось разрушение базальных ядер.
Симптоматическое лечение:
- Галюцинации, психозы — психоаналептики (Экселон, Реминил), нейролептики (Сероквель, Клозапин, Азалептин, Лепонекс)
- Вегетативные нарушения – слабительные средства при запорах, стимуляторы моторики ЖКТ (Мотилиум), спазмолитики (Детрузитол), антидепрессанты (Амитриптилин)
- Нарушение сна, боли, депрессия, тревожность – антидепрессанты (ципрамил, иксел, амитриптилин, паксил) золпидем, успокоительные средства
- Снижение концентрации внимания, нарушения памяти – Экселон, Мемантин-акатинол, Реминил
Выбор метода лечения зависит от тяжести заболевания и состояния здоровья, и осуществляется только врачом после того как проведена полная диагностика болезни Паркинсона.
Хирургическое лечение
Успехи консервативных методов лечения, несомненно, значительны и очевидны, однако возможности их, как показывает практика, не безграничны. Необходимость поиска нового в лечении болезни Паркинсона заставила задуматься над этим вопросом не только неврологов, но и врачей хирургического профиля. Достигнутые результаты, хотя их нельзя считать окончательными, уже начинают обнадеживать и радовать.
В настоящее время уже хорошо освоены деструктивные операции. К ним относятся такие вмешательства, как таламотомия, эффективная в случаях, где главным симптомом выступает тремор, и паллидотомия, основным показанием которой являются двигательные расстройства. К сожалению, наличие противопоказаний и высокий риск осложнений не позволяет широко использовать данные операции.
К прорыву в борьбе с паркинсонизмом привело внедрение в практику радиохирургических методов лечения.
Нейростимуляция, представляющая собой малоинвазивное хирургическое вмешательство — вживление стимулятора (нейростимулятора), похожего на искусственный водитель ритма (сердечный кардиостимулятор, но только для мозга), который так хорошо знаком некоторым пациентам, производится под контролем МРТ (магнитно-резонансная томография). Стимуляция электрическим током ответственных за двигательную активность глубинных мозговых структур, дает надежду и основания рассчитывать на эффективность подобного лечения. Однако в ней тоже обозначились свои «плюсы» и «минусы.
К плюсам нейростимуляции можно отнести:
- Безопасность;
- Довольно высокую эффективность;
- Обратимость (в отличие от деструктивных операций, которые являются необратимыми);
- Хорошую переносимость больными.
К недостаткам причисляют:
- Большие материальные затраты для семьи пациента (операция не всем «по карману»);
- Поломки электродов, замена генератора через несколько лет эксплуатации;
- Риск инфицирования (небольшой – до 5%).
Нейростимуляция мозга
Это новый и достаточно обнадеживающий метод лечения не только болезни Паркинсона, но и эпилепсии. Суть данной методики сводится к тому, что больному в мозг вживляют электроды, которые соединяют с нейростимулятором, установленным подкожно в области груди.
Нейростимулятор подает на электроды импульсы, что приводит к нормализации мозговой деятельности, в частности, тех структур, которые ответственны за появление симптомов болезни Паркинсона. В развитых странах методика нейростимуляции активно применяется и дает великолепные результаты.
Лечение с применением стволовых клеток
Результаты первых испытаний по применению стволовых клеток при болезни Паркинсона были опубликованы в 2009 году.
Согласно полученным данным, через 36 месяцев после введения стволовых клеток положительный эффект отмечен у 80 % больных. Лечение заключается в трансплантации нейронов, полученных в результате дифференцировки стволовых клеток, в головной мозг. Теоретически они должны заменить погибшие дофаминсекретирующие клетки. Метод на вторую половину 2011 года исследован недостаточно и не имеет широкого клинического применения.
В 2003 году впервые человеку с болезнью Паркинсона в субталамическое ядро были введены генетические векторы, содержащие ген, ответственный за синтез глутаматдекарбоксилазы. Данный фермент снижает активность субталамического ядра. Вследствие этого он оказывает положительное терапевтическое воздействие. Несмотря на полученные хорошие результаты лечения, на первую половину 2011 года методика практически не применяется и находится в стадии клинических исследований.
Перспективы растворения телец Леви
Многими исследователями считается, что тельца Леви являются не просто маркером болезни Паркинсона, но и одним из патогенетических звеньев, то есть усугубляют симптомы.
В исследованиях Assia Shisheva 2015 года показано, что агрегацию α-синуклеина с образованием телец Леви предотвращает комплекс белков ArPIKfyve и Sac3, который даже может способствовать расплавлению этих патологических включений. На основе указанного механизма появляется перспектива создания лекарства, способного растворять тельца Леви и лечить ассоциированные с ними деменции.
От чего зависит продолжительность жизни страдающих болезнью Паркинсона?
Продолжительность жизни людей с болезнью Паркинсона зависит от своевременной постановки диагноза и эффективности лечения. При обнаружении заболевания на ранних стадиях, эффективного медикаментозного лечения, соблюдения диеты и правильного образа жизни, а также при регулярном проведении различных физиопроцедур (массаж, гимнастика) продолжительность жизни практически не изменяется.
Профилактика
Людям, чьи родственники страдали этим заболеванием, нужна профилактика. Она заключается в следующих мерах.
- Нужно избегать и своевременно лечить недуги, которые способствуют развитию паркинсонизма (интоксикация, болезни мозга, травмы головы).
- От экстремального спорта рекомендуется отказаться вовсе.
- Профессиональная деятельность не должна быть связана с вредным производством.
- Женщины должны следить за содержанием эстрогена в организме, поскольку оно со временем либо после гинекологических операций снижается.
- Наконец, развитию патологии может поспособствовать гемоцистеин – высокий уровень аминокислоты в организме. Для снижения ее содержания человек должен принимать витамин В12 и фолиевую кислоту.
- Человеку нужно умеренно выполнять физические упражнения (плавать, бегать, танцевать).
В итоге отметим, что одна чашка кофе ежедневно также может помочь в защите от развития патологии, что не так давно было обнаружено исследователями. Дело в том, что под действием кофеина в нейронах вырабатывается вещество дофамин, которое укрепляет механизм защиты.
Прогноз — сколько с ней живут?
Иногда можно услышать такой вопрос: «болезнь Паркинсона, последняя стадия — сколько живут?». При этом болезни смертельный исход наблюдается от интеркуррентных заболеваний. Поясним на примере. Есть болезни, само течение которых приводит к смерти, например, перитонит, или кровоизлияние в ствол мозга. А есть заболевания, которые приводят к глубокой инвалидности, но к смерти не приводят. При надлежащем уходе пациент может жить годами, даже при переходе на зондовое питание.
Причинами смерти являются следующие состояния:
- Гипостатическая пневмония с развитием острой дыхательной, а затем и сердечно-сосудистой недостаточности;
- Появление пролежней с присоединением вторичной инфекции и сепсисом;
- Привычные запоры, парез кишечника, аутоинтоксикация, сосудистый коллапс.
Если за пациентом грамотно ухаживать, то он может прожить годы, даже будучи прикованным к постели. Вспомните пример премьер – министра Ариэля Шарона, который перенес тяжелый инсульт в 2006 году, и умер, не приходя в сознание спустя 8 лет, в январе 2014 года. Он находился в коме 8 лет, и лечение было прекращено по просьбе родственников, когда ему исполнилось 86 лет. Поэтому вопрос о поддержании жизни пациента с паркинсонизмом решается просто – это уход и поддержка, так как болезнь не ведет к непосредственной гибели больного.




Пока лишь 1 комментарий